氏名:杉本 智恵
科学技術振興機構・CREST
氏名:森 一泰
国立感染症研究所 エイズ研究センター、
(独)医薬基盤研究所 霊長類医科学研究センター
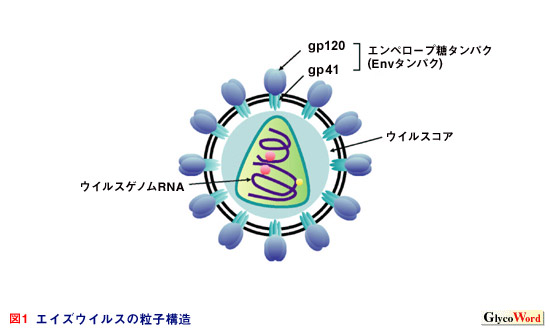
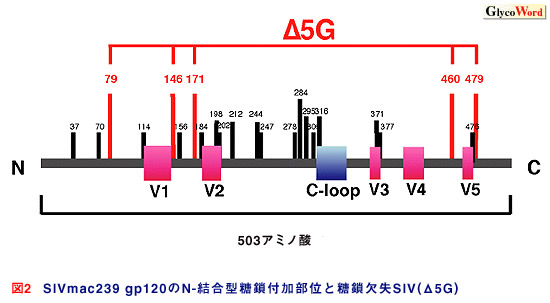
エイズウイルスの外膜スパイクタンパクEnvは、gp120とgp41という2つの糖タンパクから構成されている(図 1)。gp120は他のウイルスのスパイクタンパクと比較してきわめて糖の含有量が高く、約500アミノ酸の長さに22〜26本のN-結合型糖鎖が付加している(図 2)。この糖鎖に覆われているEnvの構造は、宿主免疫応答においてはウイルス感染制御に障害を与え、標的細胞に対してはウイルスの吸着、侵入に必要な性質を与えている。
宿主免疫応答からの回避
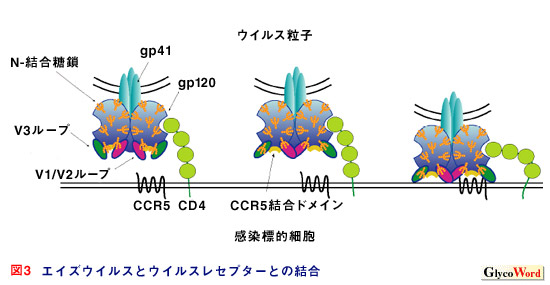
gp120は2つのウイルスレセプター(CD4とCCR5やCXCR4などのコレセプター)と結合する(図 3)。Envは中和抗体のターゲットになるはずである。しかし、表面に露出しているタンパク部分のほとんどが糖鎖構造で覆われている上に、ループ構造などのタンパク立体構造によってウイルス侵入に重要であるコレセプター結合部位はCD4と結合する前は隠されているので、エイズウイルス感染においては中和抗体ができにくい。遮蔽している糖鎖を欠失することにより、感染宿主で中和抗体誘導が改善すること1、糖鎖付加部位の場所が変わることによって、宿主に誘導された中和抗体から免疫回避した変異株が出現することも報告されている2。
ウイルスの病原性の決定
サルのエイズウイルスであるSIVのgp120には23カ所のN-結合型糖鎖付加部位が存在する。我々はそのうちの5か所にアミノ酸変異を導入して糖鎖を欠失させた変異株を作った(図 2)。この糖鎖欠失SIV(Δ5G)はサル末梢血リンパ球を用いたin vitroでの増殖性は親株と変わらなかった 3。そしてアカゲザルへの感染実験を行ってin vivoでのウイルス感染性と宿主応答の解析を行った 4。親株をアカゲザルに接種すると、感染後2週目に血中ウイルス量はピークになり、その後も持続的な高いウイルス増殖が見られ、2年ほどでエイズを発症する。しかしΔ5G感染ザルでは、感染ピークは親株の感染と同等であったにもかかわらず、その後の血中ウイルス量は検出感度以下であった 4。Δ5Gの感染制御の理由は前項のような糖鎖による免疫応答の回避から考えると、中和抗体誘導とリンクすると考えられたが、Δ5G感染ザルには必ずしも中和抗体は検出されず、細胞性免疫だけが誘導されているサルもいた。この結果から、糖鎖欠失は免疫源性を向上させるだけでなく、感染細胞の違いなどのウイルス学的性質の変化も起こすと考えられた。
ウイルスの細胞指向性の決定
Δ5Gはウイルス学的性質の解析によりマクロファージ指向性とCD4非依存性を獲得していることが明らかになった。強毒株SIVはT細胞指向性ウイルスで、ウイルスレセプターとしてCD4とCCR5を必要とし、マクロファージでは増殖できない。このような細胞指向性は標的細胞でのウイルスレセプターの発現量とレセプターの使い方で決定される。すなわちT細胞指向性ウイルスはCD4とCCR5を使用して、それらが両方とも発現するT細胞で感染・増殖できるのに対し、マクロファージ指向性ウイルスはCCR5しか発現していないマクロファージでも増殖できる。すなわちマクロファージ指向性ウイルスはCD4が存在しなくても感染できる性質(CD4非依存性)を持っている。そのように考えると、糖鎖欠失による細胞指向性の変化は、サル体内での感染細胞や感染組織を変えているかもしれない。
糖鎖欠失ウイルスとワクチンへの応用
Δ5G感染ザルに病原性SIVをチャレンジ感染させるとその感染を防御する。現在のところ、実験的に最も効果のあるエイズワクチンは弱毒生ワクチンである。しかし、これまでの遺伝子の一部を欠損した弱毒株は長期の感染によって病原性が復活することが明らかになり、弱毒生ワクチンは安全面で大きな問題を抱えている。Δ5Gはこれまでの弱毒株よりさらに病原性は低下しているにもかかわらず、同等のワクチン効果は有している。糖鎖欠失ウイルスを即エイズワクチンに利用するにはまだ多くの関門があるが、糖鎖欠失ウイルスの感染防御機構をより詳細に解析していくことにより、新たなワクチン戦略も生まれてくるかもしれない。