Apr. 01, 2026
鈴木 匡
氏名:鈴木 匡
理化学研究所 開拓研究所 鈴木糖鎖代謝生化学研究室 主任研究員
1997年東京大学大学院理学系研究科生物化学専攻 博士課程修了(博士(理学);指導教官:井上康男教授 および榎森康文助教授)。同年7月より米国ニューヨーク州立大学ストーニーブルック校ポスドク研究員(ウィリアム J. レナーツ教授)。その後研究科学者、研究助教授を経て2001年12月にJSTさきがけ研究21研究者として帰国。2002年2月より東京大学理学部で科学技術振興特任教員;2004年1月より大阪大学医学部にて特任助教授(2007年4月より特任准教授);2007年10月より理化学研究所システム糖鎖生物学研究グループ 糖鎖代謝学研究チーム チームリーダー。2018年4月より現職。
タンパク質のアスパラギン(N)結合型糖鎖は、真核細胞だけでなく、バクテリアや古細菌にも見られる最も普遍的なタンパク質の修飾機構の一つであり、その反応はオリゴ糖転移酵素(OST)によって担われる。バクテリアや古細菌では活性サブユニット単独で機能をすることが多いが、真核細胞では生物種ごとに異なるサブユニット構造をとることが知られている。最近、OSTは糖鎖をタンパク質に転移するだけでなく、ドナー基質(ドリコール結合糖鎖; DLO)の加水分解により遊離糖鎖を生成することが明らかになってきた。この加水分解反応は出芽酵母の酵素に比べて哺乳動物の酵素で著しく亢進しており、遊離糖鎖を効率的に生成できるように進化してきた、と考えることも出来る。ここではOSTについて概説するとともに、その加水分解反応の意義について仮説を提唱したい。
1. イントロダクション
オリゴ糖転移酵素(OST)はあらかじめ脂質上に作られた糖鎖(出芽酵母(Saccharomyces cerevisiae)とヒトでは14糖(Glc3Man9GlcNAc2; https://www.glycoforum.gr.jp/article/06A5J.htmlを参照))を決まった配列(sequonと呼ばれる:Asn-Xaa-Ser/Thr; XaaはPro以外の任意のアミノ酸)上に転移する酵素である。真核細胞では、OSTは小胞体(ER:Endoplasmic reticulum)に局在し、翻訳中のタンパク質に転移する共翻訳反応のほか、タンパク質が翻訳を完了した後におこる翻訳後反応を担う場合もある。糖鎖修飾はタンパク質の物性や生理機能に多大な影響を及ぼし、その遺伝子変異は糖鎖合成不全症(CDG)と総称される遺伝子疾患を引き起こすことが知られている1。昨今のクライオ電顕技術の発展により、OSTの基質認識や反応機構について多くのことがわかってきたが、その詳細については最近の総説を参照してほしい2,3。
2. OSTのサブユニット・サブ複合体構成
OSTは哺乳動物や出芽酵母中では多くのサブユニットからなる複合体であることが知られているが、生物種によっては活性サブユニットのみを持つものも知られている。例えば、Leishmania majorでは活性サブユニット以外のサブユニットは存在せず、活性サブユニット単独でOSTの機能を発揮できる。一方で、L. majorは複数の活性サブユニット(LmSTT3A-D)を持っていることが知られており、おそらく異なる性質を持つOSTを保持することが本生物にとって重要であることが示唆される4。
OSTのサブユニットは主に哺乳動物と出芽酵母において詳細に解析されている。出芽酵母では8つのサブユニットからなり、3つのサブ複合体構造を持つことが知られている(図 1)。サブ複合体1はOST1とOST5、サブ複合体2はSTT3、OST4とOST3またはOST6、サブ複合体3はWBP1、SWP1とOST2からなる。STT3、WBP1、SWP1、OST1とOST2は必須遺伝子であり、OST3、OST4、OST5とOST6は非必須遺伝子である。OST3、OST6は機能的なパラログと考えられ、チオレドキシンドメインを持ち基質タンパク質とジスルフィド結合を作ることで、STT3がsequonに出会う確率を高めている、と推測されている5。STT3は実際の酵素活性を担う活性サブユニットであるが、その他のサブユニットの機能的重要性の詳細は不明な点が多い。
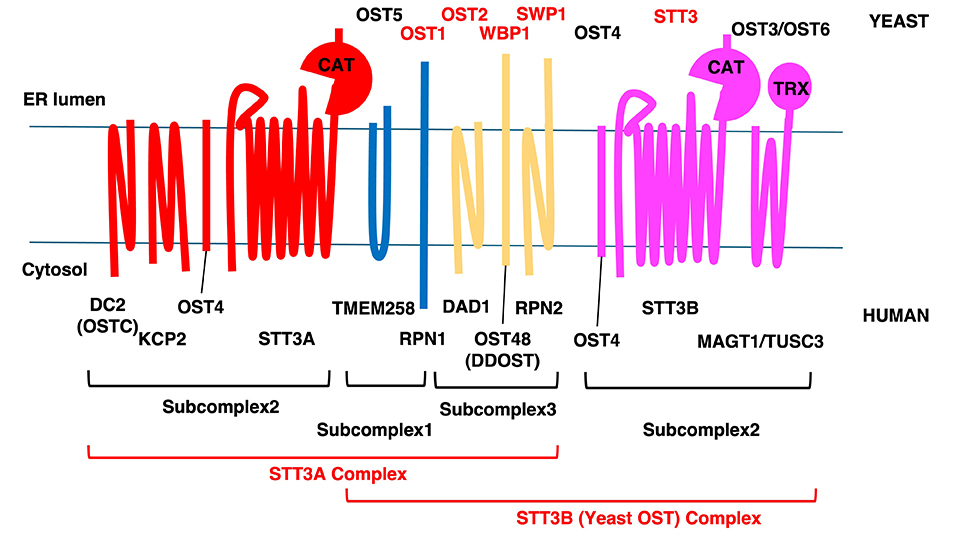 図 1. ヒトと出芽酵母(S. cerevisiae)におけるOST複合体のサブユニット構成
図 1. ヒトと出芽酵母(S. cerevisiae)におけるOST複合体のサブユニット構成
OSTは3つのサブ複合体からなる。上は酵母、下はヒトのOSTサブユニットの名前を示している。酵母のサブユニットのうち、生育に必須のタンパク質は赤で示す。STT3A複合体は翻訳と共役したOST、STT3B複合体は翻訳後に働くOSTとして機能する。酵母はSTT3B型のOSTのみを持つ。CATはSTT3AまたはBにおける活性部位、TRXはチオレドキシンドメインを示し、TRXはOST反応を促進する機能がある、と考えられている。本図は主にShrimalとGilmoreによる総説に基づいて作成した2。
3. OSTの加水分解活性
近年OSTにはドリコール糖鎖の加水分解活性があり、遊離N型糖鎖(構造上N型糖鎖の特徴を持つ遊離糖鎖; FNGs)を生成できることがわかってきた6,7(図 2)。出芽酵母OSTにおいて加水分解活性はオリゴ糖の転移活性と明確に区別できることが示されている8。哺乳動物においてOSTの加水分解活性はもっぱらSTT3B複合体によって担われている9。また、最近我々は出芽酵母OSTの加水分解活性がERストレスのような小胞体内でフォールディング不全タンパク質が増える状況で亢進されることを見出している10。我々はOSTによって生じるFNGが、タンパク質の凝集を防ぐ、あるいはフォールディングを促進するシャペロンとして機能する可能性を提唱している10。N型糖鎖によるタンパク質の凝集防止やフォールディング促進効果については、過去に生化学的に検証された例があり、一定の効果が認められている11,12。
興味深いことに、哺乳動物のOSTの加水分解活性は出芽酵母のOSTと比べ格段に活性が高く(細胞あたりのOSTによる遊離糖鎖の生成量は、出芽酵母と比べて約1万倍にもなる7)、哺乳動物においてOSTは進化的に何らかの必要性があってこの加水分解活性を発達させてきたことが伺える。その点、血清中のFNGsの存在は注目に値する13。これらのFNGsの分泌にOSTが少なくとも部分的に関与していることが示されている14。FNGsはサケの血清にもみられることから、血清遊離糖鎖は少なくとも脊椎動物において保存され、何らかの重要な役割を果たしていることが示唆される15。
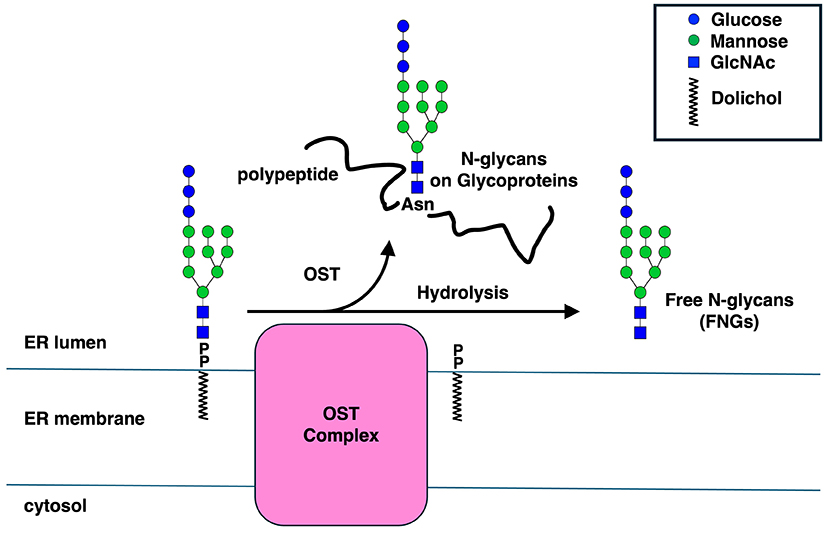 図 2. OSTの加水分解反応
図 2. OSTの加水分解反応
OSTは通常ドリコール結合糖鎖(DLO) をドナー基質としてGlc3Man9GlcNAc2の構造を持つオリゴ糖をタンパク質中の糖鎖付加配列(Sequon; Asn-X-Ser/Thr; X: Pro以外のアミノ酸)に転移する(“OST反応”)。一方、OSTはDLOを加水分解して遊離N型糖鎖(FNGs)も生成できる(“加水分解反応”)。 酵母のOSTに比べて、哺乳動物のOSTの加水分解反応の効率は格段に亢進していると考えられている。
References
- Ng BG, Freeze HH, Himmelreigh N, Blau N, Ferreira CR (2024) Clinical and Biochemical Footprints of Congenital Disorders of Glycosylation: Proposed Nosology. Mol Genet Metab 142, 108476. (doi: 10.1016/j.ymgme.2024.108476)
- Shrimal S and Gilmore R (2019) Oligosaccharyltransferase structures provide novel insight into the mechanism of asparagine-linked glycosylation in prokaryotic and eukaryotic cells. Glycobiology 29, 288-297 (doi: 10.1093/glycob/cwy093)
- Ramirez AS and Locher KP (2023) Structural and mechanistic studies of the N-glycosylation machinery: from lipid-linked oligosaccharide biosynthesis to glycan transfer. Glycobiology 33, 861-872 (doi: 10.1093/glycob/cwad053)
- Nasab FP, Schulz BL, Gamarro F, Parodi AJ and Aebi M (2008) All in one: Leishmania major STT3 proteins
substitute for the whole oligosaccharyltransferase complex in Saccharomyces cerevisiae. Mol Biol Cell 19, 3758-3768. (doi:10.1091/mbc.E08-05-0467)
- Shulz BL, Stirnimann CU, Grimshaw JPA, Brozzo MS, Fritsch F, Mohorko E, Capitani G, Glockshuber R, Grütter MG, and Aebi M (2009) Oxidoreductase activity of oligosaccharyltransferase subunits Ost3p and Ost6p defines site-specific glycosylation efficiency. Proc Natl Acad Sci USA 106 , 11061-11066. (doi: 10.1073/pnas.0812515106)
- Harada Y, Buser R, Ngwa EM, Hirayama H, Aebi M, and Suzuki T (2013) Eukaryotic oligosaccharyltransferase generates free oligosaccharides during N-glycosylation. J Biol Chem 288, 32673-32684. (doi: 10.1074/jbc.M113.486985)
- Harada Y, Masahara-Negishi Y, and Suzuki T (2015) Cytosolic-free oligosaccharides are predominantly generated by the degradation of dolichol-linked oligosaccharides in mammalian cells. Glycobiology 25, 1196-1205 (doi: 10.1093/glycob/cwv055)
- Yamasaki T and Kohda D (2020) Uncoupling the hydrolysis of lipid-linked oligosaccharide from the oligosaccharyl transfer reaction by point mutations in yeast oligosaccharyltransferase. J Biol Chem 295, 16072-16085 (doi: 10.1074/jbc.RA120.015013)
- Lu H, Fermaintt CS, Cherepanova NA, Gilmore R, Yan N, and Lehrman MA (2018) Mammalian STT3A/B oligosaccharyltransferases segregate N-glycosylation at the translocon from lipid-linked oligosaccharide hydrolysis. Proc Natl Acad Sci USA 115, 9557-9562 (doi: 10.1073/pnas.1806034115)
- Li ST, Hirayama H, Huang C, Matsuda T, Oka R, Yamasaki T, Kohda D, and Suzuki T (2024) Hydrolytic activity of yeast oligosaccharyltransferase is enhanced when misfolded proteins accumulate in the endoplasmic reticulum. FEBS J 291, 884-896 (doi: 10.1111/febs.17011)
- Kimura N, Uchida M, Nishimura S, and Yamaguchi H (1998) Promotion of polypeptide folding by interactions with Asn-Glycans. J Biochem 124, 857-862 (doi: 10.1093/oxfordjournals.jbchem.a022190)
- Kosaka S, Katsube M, Maeda M, and Kimura Y (2022) Improved method for preparation and purification of recomninant α-synuclein: high-mannose-type free N-glycan prepared from an edible bean (Vigna angulari, Azuki bean) inhibits α-synuclein aggregation. Biosci Biotechnol Biochem 86, 770-774 (doi: 10.1093/bbb.zbac040)
- Huang C, Honda A, and Suzuki T (2025) Free oligosaccharides in serum. BBA Adv 7, 100139 (doi: 10.1016/j.bbadva.2025.100139)
- Huang C, Seino J, Honda A, Fujihira H, Wu D, Okahara K, Kitazume S, Nakaya S, Kitajima K, Sato C, and Suzuki T (2024) Rat hepatocytes secrete free oligosaccharides. J Biol Chem 300, 105712 (doi: 10.1016/j.jbc.2024.105712)
- Honda A, Seino J, Huang C, Nakano M and Suzuki T (2025) Occurrence of free glycans in salmonid serum. Biochem Biophys Res Commun 742, 151096 (doi: 10.1016/j.bbrc.2024.151096)


