
氏名:大塚 英典
東京理科大学理学部第一部応用化学科教授
東京理科大学大学院理学研究科化学専攻博士課程修了 博士(理学)取得、1995年 日本チバガイギー(株)((現)Novartis Japan)。その後、東京大学大学院/東京女子医科大学にて日本学術振興会特別研究員、国立研究開発法人産業技術総合研究所(AIST)研究員、国立研究開発法人物質材料研究機構(NIMS)主幹研究員、2006年 東京理科大学理学部第一部応用化学科助教授を経て現職。界面コロイド化学を駆使した生体機能性界面材料の研究に従事~血液適合性の高い高分子表面、レドックス活性の高い高分子型錯体・金属ナノ粒子の合成と標的型DDS、細胞の三次元ゲル培養と組織工学・再生医療への展開。
再生医療における組織工学的アプローチとして、細胞を三次元に培養する際の足場となる、新たなハイドロゲルを開発し、簡便に合成する手法を確立した。ここでハイドロゲルとは、高分子の鎖が形成するネットワークが水などの液体を含んだものを意味する。生体内では、細胞はさまざまな生体高分子から形成される細胞外基質(extracellular matrix: ECM)を足場として増殖・分化するため、体外で細胞培養を行う際も、足場となる材料が必要となる。近年、ECMを模倣した材料として、相互侵入高分子網目構造(interpenetrating polymer network: IPN)と呼ばれる、複数の高分子が互いに絡み合って、独立に多重の網目構造を形成するハイドロゲルが、注目されている。
キトサンは高い生体適合性、生分解性を有するバイオマテリアルとしてよく利用されているため、本研究では、キトサン/ポリエチレングリコール/自己会合性ペプチドからなる相互侵入高分子網目ハイドロゲル(以後、IPNゲル)を細胞足場材料として開発した。具体的には、ペプチドが自律的に繊維状のβシート構造を形成する現象(自己組織化)と、それに続くキトサンとポリエチレングリコールの共有結合形成によって、IPNネットワークを、in-situで簡便にone-pot(単一の反応容器内)合成する技術である。実際、今回開発したIPNゲルは足場材料として適した構造を持ち、かつ関節軟骨細胞がIPNゲルを足場として自律的に増殖・再生することも確認された。
関節軟骨は約2~7mm の非常に薄い組織であるが,関節機能の上で重要な役割を担っている。その組織学的構成は非常に特殊で,豊富な軟骨基質の中に軟骨細胞は2% 程度しか存在していない。また,軟骨細胞は分裂能力が低く,活動性は高くない。そのため,関節軟骨にいったん損傷が生じると,損傷治癒機転が働きづらく自己修復に乏しい。外傷に伴う軟骨欠損や,離断性骨軟骨炎,変形性関節症などで発生した軟骨病変に対しては有効な治療方法がないのが現状である。
その対処アプローチとしてTissue Engineering の発展に高い期待が寄せられている。現在までに自家軟骨移植,自家細胞移植などが行われているが,一つの問題点として,使用するドナーである自家の年齢があげられる。特に関節症の治療においては多くが高齢者であり,高齢に伴う軟骨基質合成の年代的限界とこれを構成するヒアルロン酸の分子量の低下が課題視されている。本研究で開発された新しい細胞足場材料の合成技術は、超高齢化社会を迎える現代において、軟骨再生医療の進展に重要な役割を果たすことが期待される。さらに、免疫拒絶反応が起こるリスクもなかったという点でも、極めてニーズが高い医療技術である。
関節軟骨は硝子軟骨からなり、この組成は水分が約80%、コラーゲンが12%、プロテオグリカンとヒアルロン酸が2%,その他が約6%で、軟骨細胞は軟骨容量のわずか2-3%しか占めない。乾燥重量で比較した総タンパク質における割合はII型コラーゲンが約60%、アグリカンが約35%とされている。
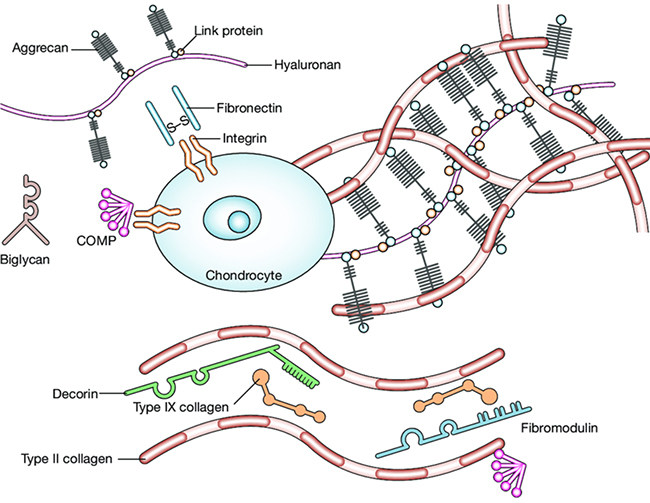
軟骨マトリックスは、コラーゲンから成る線維成分とその間隙を埋めるヒアルロン酸、アグリカン等のプロテオグリカン群およびその他の糖タンパク質から構成されている。前者(第一ネットワーク)の線維成分が組織の基本骨格を構築して剛性を担う一方,後者(第二ネットワーク)は線維間に沈着して軟骨に独特の硝子様形態と弾力性を与えている。後者の主成分はアグリカンとヒアルロン酸で、これらの分子はリンクタンパク質(linkprotein,LP)とともにプロテオグリカン会合体という一定の構造を形成して組織に沈着している(Fig. 1)1,2。
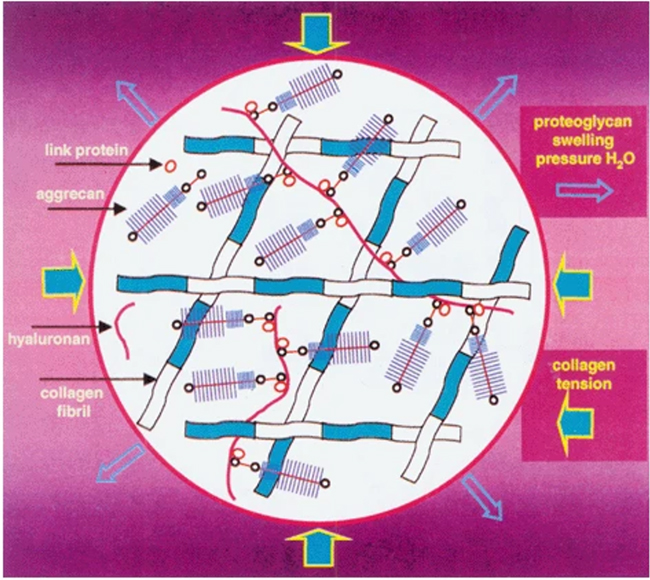
高濃度では、プロテオグリカンは大きな浸透圧による膨潤圧を生み出し、組織内に水分を引き込む。これは、アグリカンを構成するグルコサミノグリカン(GAG)鎖上の負に帯電した陰イオン基すべてが、Na+などの可動性対イオンを伴っているためである。これにより、軟骨と周囲組織の間でイオン濃度に大きな差が生じ、自由に拡散する陰イオンと陽イオンの間に不均衡が生じる。この浸透圧の不均衡と、アグリカンの分子が大きすぎて再分布できない性質により、水分が軟骨内に引き込まれる。水分の増加により、アグリカン豊富な基質ネットワークは膨潤・拡張する。この水分で膨潤した基質は、軟骨の生物力学的特性に極めて重要である。コラーゲン網目構造はアグリカンのマトリックス内での移動能力を著しく圧縮制限する結果、膨張圧力を生みだす。複合的なコラーゲン/アグリカンネットワーク自体が剛性が高く変形に抵抗する性質を持つ点はもう一つの重要な特徴である。アグリカンは流体の流動や水分再分布に対しても強い抵抗を示す。したがって軟骨は粘弾性組織と呼ばれ、急激な衝撃荷重に抵抗する剛性のある弾性ポリマーのように振る舞いながら、持続的な荷重下では遅延した非弾性変形を示す特性を有する(Fig. 2)3。
我々の体を構成する ECM は多種多様の生体高分子ネットワークから形成されている。欠陥組織の再生を試みる場合,細胞を生体内のECM 構造に類似した材料と共に移植することで,構造的にも機能的にも目的としている臓器の特徴を保持した組織が効率的に再生されるものと期待できる。したがって,組織再生にはECM 構造を再現した細胞足場剤,特にハイドロゲルの開発が急務である。生体構成ECMの一つであるコラーゲンやヒアルロン酸のような生物由来のハイドロゲルは生理活性が高い反面、機械的強度が不十分である。そこでin vivo での寿命と強度向上に向けて、生体にみられるコラーゲンとヒアルロン酸が形成する複合ネットワークを手本に、ゲルマトリックスへの第二ネットワークの導入を検討した。
IPN は,異種の高分子ネットワークが互いに独立に存在する材料であり,ハイドロゲルの生物学的および物理的な特性を精密に制御かつ相乗的な高機能化が可能な構造化材料である4-6。生体由来材料の機能を保持したまま、その欠点を補う合成材料との融合は,物理的からみ合いと共有結合性の架橋のいずれによって行うこともできる。しかし,ここで生じる問題点が,「このネットワーク構造をどの様に構築するか」である。一般的なIPNゲルの作製方法は、一つのネットワークを作り上げた後、追加のネットワークを光照射や他の化学物質を添加するなど、多くの場合は外部刺激が必要である。この手法でのネットワーク形成は多段階処理を要し、さらに細胞毒性を与えるラジカル種を発生するなど、組織再生に向けた足場材料の構築には適さない。したがって、医療への応用、特にTissue Engineeringへの応用を考えた場合、欠陥患部へ直接注入し代替材料を作製することが理想的である。仮に注入するだけで自発的にIPN ゲルを作製できれば、施術後のquality of life を高く維持でき、何より効率的に軟骨組織を再生可能な低侵襲治療の実現を叶えるであろう。つまり、足場材料作製において重視すべきポイントは、生体内環境を模倣したIPN 構造を、外部刺激なくインジェクタブル形式で作製することにある。
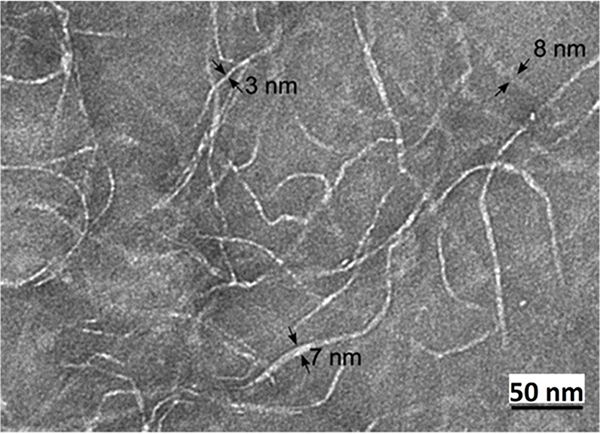
インジェクタブルIPN ゲル作製のための着眼点は,「異種ネットワーク間における”架橋の駆動力”と“ゲル化速度のタイムラグ”を巧みに利用することにより、インジェクタブルシステムで生分解性IPN ゲルの構造化を可能とする」点にある。そこで我々は、自己組織化ペプチド(RADA16) とキトサン(CH)-PEG (CH/PEG) の両ネットワークを選択した。RADA16 は自己組織化ペプチドであり、塩の添加やpH の変化により分子間で静電的相互作用や疎水性相互作用を併発し、即座にβ-sheet 構造を形成するインジェクタブルゲルである(Fig. 3)7,8。
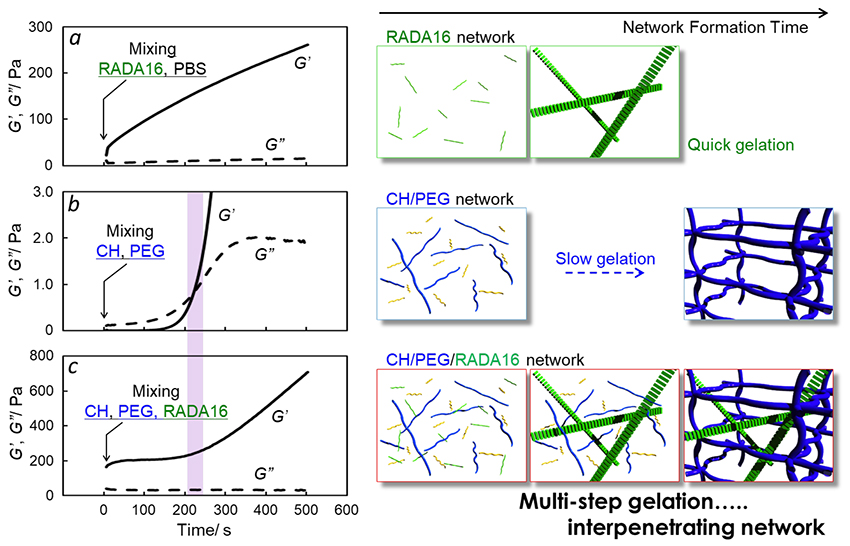
もう一方のネットワークを構成するCHは生理条件で易溶であるように調製されたCH であり、豊富なアミノ基も有している。このCH の特性を利用して、両末端スクシンイミド化PEG(NHS-PEG-NHS)とCH がアミド結合の形成に基づき架橋反応が進行することを報告している9,10。その際のゲル化は即座に完了するのではなく、一定時間経過後に粘性体のゾルから粘弾性体のゲルへとゆっくりと相転移するインジェクタブルゲルである。この様に、双方ネットワークで「ゲル化原理」と「ゲル化速度」を考えてみると、これらのゲル前駆体を混合すれば、二種ネットワークの自発的な逐次的架橋に基づき、インジェクタブルIPN ゲルをone-pot で作製できると推測される。これを実証するため、粘弾性測定によりゲル化速度を調査した。RADA16 ペプチドの場合、PBS との混和直後から、貯蔵弾性率は損失弾性率よりも高い、つまり極めて早いゲル化(第一ネットワーク)を示した。一方のCH/PEG ゲルでは、溶液混和後、所定時間経過の後に貯蔵弾性率の急激な上昇が観測され、明確なゲル化点が確認でき、RADA16 に比べると遅いゲル化(第ニネットワーク)を示すことが確認できた。これらを混ぜ合わせたCH/PEG/RADA のゲル化プロファイルにおいて、貯蔵弾性率は多段階に変化し、その変曲点のタイムスケールは、CH/PEG ゲルのゲル化点と高い相関を示した。この結果は、逐次的なネットワーク構造の形成を説明している(Fig. 4)11。
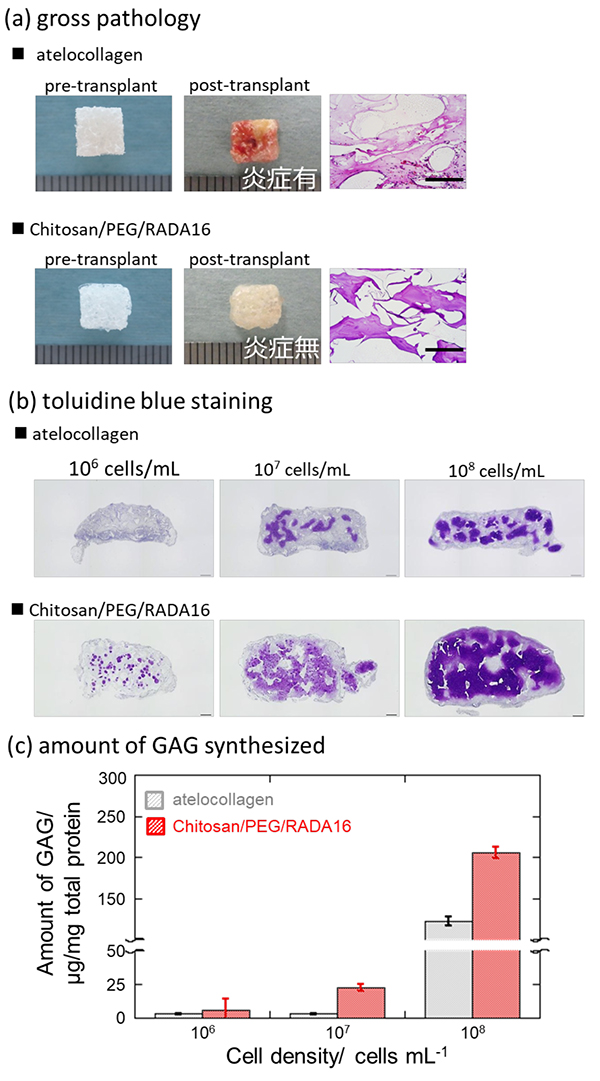
機能的には、第一ネットワークの有する組織分化能と第二ネットワークの有する高い強度を相乗増強させた細胞足場を提供した。このようなIPN ゲルの有効性は、in vivo での移植実験からも確認できた(Fig. 5)11。6週令のマウスの皮下に異なる細胞密度のヒト由来軟骨細胞を内包したゲルを注入し、8週間培養した。肉眼的病理所見において、アテロコラーゲンゲルでは移植後にはっきりとした炎症反応が認められたのに対し、IPN ゲルでは炎症が見られなかった。加えて、トルイジンブルー(TB) 染色にて軟骨基質の形成を確認した。TB染色は、結合組織(ヒアルロン酸)、軟骨基質(ムコイチン硫酸、コンドロイチン硫酸)等に存在している酸性粘液多糖類がトルイジンブルーの塩基性タール系色素に対し異調染色(メタクロマジー)を示すことを利用した染色方法である。その結果、ヒアルロン酸およびGAG の産生において、IPN ゲルではより少ない細胞数での軟骨細胞の高い分化誘導が顕著に認められ、有効なヒト軟骨の再生を促すことが分かった。
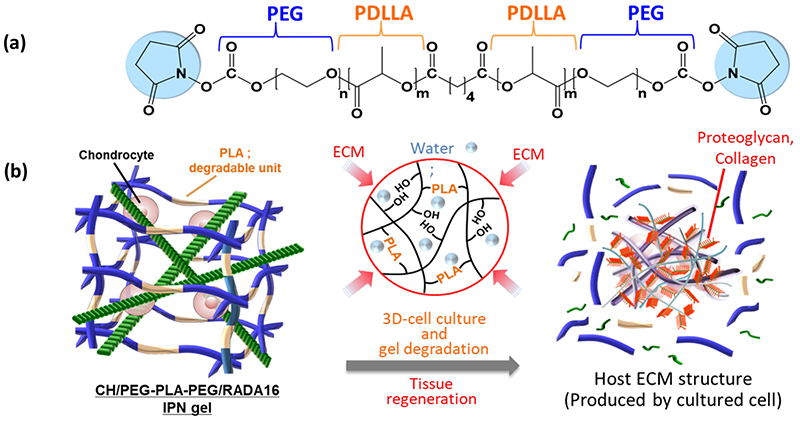
組織再生を指向するハイドロゲル足場は、ゲル内に包埋した細胞から産生されるECM を一時的に保持するコンテナとして機能し、最終的にハイドロゲルが分解することで生体由来組織に置換されることが理想である。本IPN ゲルに積極的な分解特性を付与できれば、合成のIPN 足場材料は細胞から産生されるECM との置換が生じものと期待できる。本研究では、先行のPEG 架橋剤に対し、生分解性分子としてpoly(D,L-lactide)(PDLLA)を導入したPEG-PLA-PEG(Mn≒5K)を架橋剤として用い、生分解性IPN ゲルを新規に作製した(Fig. 6)12。
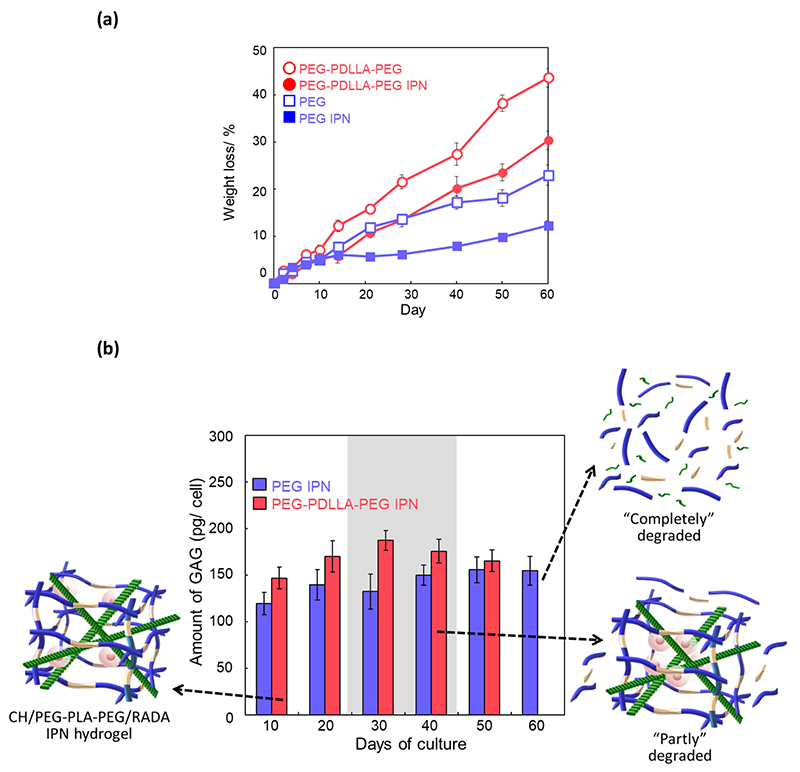
PDLLA のエステル結合に由来する加水分解に着目し、PEG架橋剤へのPLA ユニットの導入とそれに伴うゲル分解挙動を検討した。Fig. 7a は、生理条件下(37 ºC、5% CO2)において、ゲルを150 mM PBS に浸漬させた際、経過時間に対するゲルの分解挙動を示している。ここで、非分解性架橋剤として、PEG(Mn≒5K、Fig. 6)を用いた。PEG-PLA-PEG を架橋剤として用いたゲルの分解速度は、非分解性架橋剤を用いたゲルと比較し約2-3 倍加速した。双方の架橋剤において、RADA16ペプチドとのIPN化によるネットワーク強化に依存した分解挙動の遅延が観察でき、結果として8 週間に渡る緩やかなゲルの分解挙動が観察された。
組織再生を指向する場合、ハイドロゲルスキャフォールドにおける細胞封入戦略では、細胞を液体溶液中の前駆体と混合した後、ゲル化と細胞封入を行う。架橋構造は細胞により新規合成されたECMの主要構成分であるグルコサミノグリカンやコラーゲン等の拡散を大きく左右するため、スキャフォールドの分解はECM合成および巨視的組織発生に密接に追随しなければならない。ゲル前駆体、ゲル化メカニズム、分解生成物は細胞適合性を有する必要がある。「軟骨の分子機構」で述べたように、グルコサミノグリカンが持つ高保水性と含水浸透圧による膨張圧、これをコラーゲン線維が圧縮制限する結果生じる膨潤圧力、両者により軟骨の荷重が保たれる。その構造的には、コラーゲン線維とプロテオグリカン分子が相互侵入高分子網目(IPN)構造を形成し、軟骨に圧縮強さを与える。Fig. 7b に、ウシ由来初代軟骨細胞の三次元培養におけるゲル内GAG蓄積量の経時遷移を示す。分解性架橋剤用いたゲルのGAG蓄積量は、ゲルの分解に伴い向上し、かつ非分解性架橋剤を用いたゲルよりも優れていた。最終的に分解性架橋剤を用いたゲルでは約7 週間程度でゲルは分解するが、ゲルの分解に伴いGAGの蓄積効果は増加した。この結果は、Fig. 7aで示した生分解IPNがもたらす分解性向上と合わせると、生分解性IPN ゲルと産生マトリックスとの置き換わりを意味し、理想的な組織再生足場を構築できた事を示唆した。また、分解性架橋剤を用いた場合、非分解性架橋剤と比較し、関節軟骨を構成する硝子軟骨形成を示唆する因子であるcol2a1/ACAN/SOX9 遺伝子群の発現が向上していた。かつ、Fig. 5cで示したTB染色より、ヒアルロン酸およびGAGなどの酸性粘液多糖類の蓄積が認められた。つまり、分解性IPNの関節軟骨再生への適用は、軟骨ECM 産生を効率的に促すのみならず、より実関節軟骨組織に近い組織再生を実現していることを示唆する。すなわち、生分解性IPN は組織再生に伴い産生されるECM との経時置換を果たす足場として、その応用が期待される。
本IPN ゲルは、分解性架橋剤と非分解性架橋剤の混合割合を制御することで、容易に分解速度と力学強度を制御可能である。その結果、内包した薬物の放出制御や、さらに、関節軟骨組織再生のみならず、骨、皮膚、神経など、適用組織に依存した最適環境を構築可能であるため、多臓器組織再生への応用も容易である。また、従来、IPN ゲルの作製には、複数ステップの合成過程が不可欠である。これらIPN ゲルの作製には、複数のネットワークをそれぞれ単独に形成させ、複数回の操作を要する。加え、二次ネットワークの形成には細胞毒性や遺伝子損傷の原因となるラジカル種の発生を伴うため、臨床応用には適さない。しかしながら、本IPN ゲルは、特別な外部刺激条件を必要とせず、One-pot で生分解性のIPN 構造を有するインジェクタブルゲルを作製できることから、関節軟骨組織再生に代表される臨床応用への発展性に優れる。
加えて、免疫応答(毒性)に成り得るタンパク医薬品を使用せずとも、ゲル物性という培養環境のみで優れた組織再生を実現できる点にある。現存足場材料のアテロコラーゲンに比べ安全性が高く(免疫応答なし)、簡便に足場材料を作製可能である。つまり、従来の細胞移植材料に替わる汎用的な足場材料となることが期待され、再生医療において大きな進歩の礎となることが期待される。